|
|
治験依頼者の方へ |
|
本WEBサイトは、神戸メディカルクラスターの各医療機関の「治験実績」「疾患領域の特性」 「各医療機関への申請手順」などの治験に関わる情報を一元的に提供することで 治験依頼者の皆様の利便性の向上と当エリアにおける治験のさらなる活性化を目指しています。 治験を依頼する医療機関を検討される際には、ぜひ本WEBサイトをご活用ください。 また、本WEBサイトで提供する情報に関するご要望がございましたら、お気軽にお尋ねください。 |
実施中の治験 ※2024年12月末時点
- 神戸市立医療センター中央市民病院
| 治験種別 | 疾患領域 | 試験名・適応症 | 備考 |
| 医師主導治験 | 循環器内科 | Fontaine分類 IIb度の下肢閉塞性動脈硬化症の患者を対象にしたEIM-001の下肢筋肉内投与による二重盲検ランダム化比較試験 | |
| 循環器内科 | 症候性閉塞性肥大型心筋症の成人患者を対象としたmavacamtenの第3相試験 | ||
| 循環器内科 | 心血管疾患を対象としたOlpasiran (AMG 890)の第III相試験 | ||
| 循環器内科 | 急性リンパ性白血病患者を対象としたブリナツモマブの第III相試験 | ||
| 医師主導治験 | 循環器内科 | Fontaine分類Ⅲ及びⅣ度の下肢閉塞性動脈硬化症の患者を対象にしたEIM-001の下肢筋肉内投与による二重盲検ランダム化比較試験 | |
| 循環器内科 | 高リポ蛋白(a)血症患者を対象としたlepodisiranの第Ⅲ相試験 | ||
| 医師主導治験 | 脳神経内科 | 高用量E0302の筋萎縮性側索硬化症に対する第Ⅲ相試験-医師主導治験- | |
| 脳神経内科 | 遅発型ポンペ病患者を対象としたCIPAGLUCOSIDASE ALFA及びミグルスタット併用投与の拡大治験 | ||
| 脳神経内科 | 成人の慢性炎症性脱髄性多発根神経炎(CIDP)患者を対象としたNipocalimab の第Ⅱ/Ⅲ相試験 | ||
| 脳神経内科 | EFFICACY AND SAFETY OF POZELIMAB AND CEMDISIRAN COMBINATION THERAPY IN PATIENTS WITH SYMPTOMATIC GENERALIZED MYASTHENIA GRAVIS 症候性全身型重症筋無力症患者を対象としたpozelimab及びcemdisiran併用療法の有効性及び安全性 |
||
| 呼吸器内科 | ステージ I/II 非小細胞肺癌の患者を対象としたデュルバルマブの第III相試験 | ||
| 医師主導治験 | 呼吸器内科 | 進行非扁平上皮非小細胞肺癌に対するカルボプラチン+ペメトレキセド+アテゾリズマブ療法とカルボプラチン+ペメトレキセド+アテゾリズマブ+ベバシズマブ療法の多施設共同オープンラベル無作為化第Ⅲ相試験 | |
| 呼吸器内科 | 非小細胞肺癌患者を対象としたBMS-936558/BMS-734016の第Ⅲ相試験 | ||
| 呼吸器内科 | REGN2810の第1相試験 | ||
| 呼吸器内科 | 慢性閉塞性肺疾患(COPD)患者を対象としたベンラリズマブの第Ⅲ相試験 | ||
| 呼吸器内科 | 非小細胞肺癌患者を対象としたBMS-936558の第Ⅲ相試験 | ||
| 呼吸器内科 | 肺がん患者を対象としたAMG510の第Ⅲ相試験 | ||
| 呼吸器内科 | 局所進行非小細胞肺癌患者を対象としたBMS-936558/BMS-734016の第Ⅲ相試験 | ||
| 呼吸器内科 | 進行性非小細胞肺癌を有する被験者を対象として第3世代EGFR-TKI JNJ-73841937(Lazertinib)の単剤投与又はヒト二重特異性抗EGFR及びcMet抗体JNJ-61186372との併用投与における安全性及び薬物動態を評価する第1/1b相,非盲検試験 | ||
| 呼吸器内科 | TAS-115(pamufetinib)の第II相用量反応試験 | ||
| 呼吸器内科 | EGFR遺伝子変異陽性非小細胞肺がんを対象としたONO-7475の第Ⅰ相試験 | ||
| 医師主導治験 | 呼吸器内科 | KRAS G12C変異陽性の化学療法未治療進行再発の非扁平上皮・非小細胞肺癌患者を対象としたsotorasib+カルボプラチン+ペメトレキセドの第II相試験 | |
| 呼吸器内科 | オシメルチニブが無効となったEGFR変異局所進行又は転移性非小細胞肺癌患者を対象としてアミバンタマブ及びlazertinibとプラチナ製剤を含む化学療法の併用とプラチナ製剤を含む化学療法を比較する第3相、非盲検、ランダム化試験 | ||
| 呼吸器内科 | PD-L1発現で選定された、未治療の局所進行、切除不能、又は遠隔転移を伴う非小細胞肺癌患者を対象としたBGB A317-A1217-302(AdvanTIG-302)の第Ⅲ相試験 | ||
| 呼吸器内科 | 悪性腫瘍患者を対象としたマスタースクリーニング試験/局所進行切除不能Ⅲ期非小細胞肺癌患者を対象としたアレクチニブ,エヌトレクチニブ,Pralsetinibの第Ⅰ-Ⅲ相試験 | ||
| 呼吸器内科 | 非小細胞肺癌患者を対象としたSacituzumab Govitecanの第3相試験 | ||
| 呼吸器内科 | 特発性肺線維症患者を対象としたBI 1015550の第Ⅲ相試験 | ||
| 呼吸器内科 | 進行性線維化を伴う間質性肺疾患患者を対象としたBI 1015550の第Ⅲ相試験 | ||
| 呼吸器内科 | 特発性肺線維症患者を対象としたBMS-986278の有効性、安全性及び忍容性を検討する試験 | ||
| 呼吸器内科 | 進行性肺線維症患者を対象とした BMS-986278の有効性、安全性及び忍容性を検討する試験 | ||
| 呼吸器内科 | 増悪歴を有する症候性の慢性閉塞性肺疾患(COPD)患者を対象としたトゾラキマブの有効性及び安全性試験(MIRANDA) | ||
| 呼吸器内科 | A Randomized, Multicenter, Open-label, Phase III Study of Lurbinectedin Single-Agent or Lurbinectedin in Combination with | ||
| 呼吸器内科 | A randomized, phase 3, open-label study to evaluate SGN-B6A compared with docetaxel in adult subjects with previously treated | ||
| 呼吸器内科 | 特発性肺線維症及び進行性肺線維症患者を対象としたBI 1015550の非盲検継続投与試験 | ||
| 呼吸器内科 | Uncommon EGFR 遺伝子変異陽性非小細胞肺癌患者を対象としたアファチニブ投与における DFP-14323 を併用した際の有効性を検証する臨床第 III 相試験 | ||
| 呼吸器内科 | 非小細胞肺癌の患者を対象としたMK-2870の第Ⅲ相試験 | ||
| 呼吸器内科 | 特発性肺繊維症を対象とした第2b/3相試験 | ||
| 血液内科 | 未治療のびまん性大細胞型B細胞リンパ腫患者を対象としたポラツズマブ ベドチンとR-CHP併用療法の有効性及び安全性をR-CHOP併用療法と比較する第III相試験 | ||
| 血液内科 | ハイリスクのくすぶり型多発性骨髄腫患者を対象にダラツムマブの皮下投与と積極的経過観察を比較検討する第3 相ランダム化多施設共同試験 | ||
| 血液内科 | 造血幹細胞移植による初回治療が予定されていない未治療の多発性骨髄腫患者を対象にダラツムマブ,ボルテゾミブ,レナリドミド,及びデキサメタゾン併用(D-VRd)とボルテゾミブ,レナリドミド,及びデキサメタゾン併用(VRd)を比較する第3相試験 | ||
| 血液内科 | 未治療マントル細胞リンパ腫患者に対するAcalabrutinibの第Ⅲ相試験 | ||
| 血液内科 | 日本人の成熟B細胞性悪性腫瘍患者を対象としたzanubrutinibの第I/II相試験 | ||
| 血液内科 | 骨髄異形成症候群患者を対象としたベネトクラクスの第Ⅲ相試験 | ||
| 血液内科 | INCB050465(Parsaclisib)の第2相試験 A Phase 2 study of INCB050465 (Parsaclisib) at the request of Incyte Biosciences Japan G.K. | ||
| 血液内科 | 造血幹細胞移植(HSCT)後に血栓性微小血管症(TMA)を呈する患者を対象としたラブリズマブの第Ⅲ相試験 | ||
| 血液内科 | Therapy in Subjects with Relapsed/Refractory Myelofibrosis (TRANSFORM-2)再発/難治性骨髄線維症患者を対象にnavitoclaxとルキソリチニブの併用投与の有効性及び安全性を利用可能な最良の治療と比較評価する無作為化非盲検第Ⅲ相試験(TRANSFORM-2) | ||
| 血液内科 | CTL019の第Ⅲb相試験 | ||
| 血液内科 | びまん性大細胞型B細胞リンパ腫患者を対象とした第III相試験 | ||
| 血液内科 | マントル細胞リンパ腫患者を対象としたLOXO-305の第3相試験 | ||
| 血液内科 | A Phase 1 Study of JNJ-64007957, a Humanized BCMA x CD3 Bispecific Antibody in Japanese Patients with Relapsed or Refractory Multiple Myeloma 再発又は難治性多発性骨髄腫を有する日本人患者を対象としたヒト化BCMA×CD3二重特異性抗体JNJ-64007957の第1相試験 第Ⅰ相試験 |
||
| 血液内科 | 製品規格に適合しないLISOCABTAGENE MARALEUCELを被験者に投与する拡大アクセス試験(EAP) | ||
| 血液内科 | 未治療CD20陽性B細胞性濾胞性リンパ腫患者を対象としたIDEC-C2B8-SCの臨床第Ⅲ相試験 | ||
| 血液内科 | 再発/難治性濾胞性リンパ腫患者及び辺縁帯リンパ腫患者を対象としたINCMOR00208の第3相試験 | ||
| 血液内科 | 慢性移植片対宿主病を対象としたME3208の第III相試験 | ||
| 血液内科 | B細胞性非ホジキンリンパ腫患者を対象としたREGN1979の第Ⅱ相試験 | ||
| 血液内科 | 初発のフィラデルフィア染色体陽性の慢性期慢性骨髄性白血病患者を対象としたABL001の第Ⅲ相試験 | ||
| 血液内科 | 再発又は難治性の多発性骨髄腫患者を対象としたヒト化GPRC5D×CD3二重特異性抗体talquetamabの第1/2相,first-in-human,非盲検,用量漸増試験 | ||
| 血液内科 | 再発又は難治性(R/R)B 細胞性非ホジキンリンパ腫(B-NHL)を対象としたツシジノスタットとリツキシマブ併用の第 Ib/II 相試験 | ||
| 血液内科 | 慢性特発性血小板減少性紫斑病を有する日本人成人患者を対象として血小板減少症の治療におけるavatrombopagの有効性及び安全性を評価する非盲検試験 | ||
| 血液内科 | 多発性骨髄腫患者を対象としたベネトクラクスの第Ⅲ相試験 | ||
| 血液内科 | A Phase 3, Randomized, Open-Label Study to Evaluate Safety and Efficacy of Epcoritamab in Combination with R-CHOP Compared to R-CHOP in Subjects with Newly Diagnosed Diffuse Large B-Cell Lymphoma (DLBCL) 初発のびまん性大細胞型B 細胞リンパ腫(DLBCL)患者を対象とした,エプコリタマブとR-CHOP の併用療法の安全性及び有効性をR-CHOP 療法と比較する第III 相,無作為化,非盲検試験 |
||
| 血液内科 | 温式自己免疫性溶血性貧血を対象としたVAY736の第Ⅲ相試験 | ||
| 血液内科 | パルサクリシブ (INCB050465)を継続投与する第Ⅱ相試験 | ||
| 血液内科 | 再発又は難治性のびまん性大細胞型 B 細胞リンパ腫を対象としたMT-2111の第Ⅲ相試験 | ||
| 血液内科 | 同種造血細胞移植(同種HCT)を受ける急性骨髄性白血病(AML)患者に対する補助療法及び維持療法としてのMocravimodの有効性及び安全性を評価するための前向き、ランダム化、二重盲検、プラセボ対照、多施設共同第III 相試験 | ||
| 血液内科 | Expanded Access Study for the Treatment of Patients with Commercially Out-of-Specification Axicabtagene Ciloleucel 製品規格外Axicabtagene Ciloleucelを用いた患者治療のための拡大アクセス試験(EAP) |
||
| 血液内科 | A Phase 3, Open-Label Study to Evaluate Safety and Efficacy of Epcoritamab in Combination with Rituximab and Lenalidomide (R2) compared to R2 in Subjects with Relapsed or Refractory Follicular Lymphoma (EPCORE™ FL-1) 再発又は難治性の濾胞性リンパ腫被験者を対象として,エプコリタマブとリツキシマブ + レナリドミド(R2)療法を併用投与したときの安全性及び有効性をR2療法と比較評価する第III相非盲検試験(EPCORE™ FL 1) |
||
| 血液内科 | 多発性骨髄腫患者を対象としたエルラナタマブ(PF-06863135)の第Ⅲ相試験 | ||
| 血液内科 | 未治療の大細胞型リンパ腫患者を対象としたRO7082859(Glofitamab)の第Ⅲ相試験 | ||
| 血液内科 | CLL/SLL患者を対象としたMK-1026の第Ⅲ相試験 | ||
| 血液内科 | T 細胞リンパ腫患者を対象としたBMS 986369 の第1 /2 相試験 | ||
| 血液内科 | 慢性移植片対宿主病を対象としたAxatilimabの第Ⅲ相試験 | ||
| 血液内科 | 本態性血小板血症患者を対象としたMK-3543の第Ⅲ相試験 | ||
| 血液内科 | 未治療の濾胞性リンパ腫を対象としたエプコリタマブ+ R2 療法の併用療法と免疫化学療法の比較試験 | ||
| 腫瘍内科 | 食道がん患者を対象としたニボルマブとイピリムマブの第Ⅲ相試験 | ||
| 腫瘍内科 | 胃腺癌及び食道胃接合部腺癌を対象としたMK-3475の第Ⅲ相試験 | ||
| 腫瘍内科 | 胃癌を対象としたMK-3475の第Ⅲ相試験 | ||
| 腫瘍内科 | 結腸・直腸癌患者を対象としたMK-7902/E7080(レンバチニブ) とMK-3475(ペムブロリズマブ)の第Ⅲ相試験 | ||
| 腫瘍内科 | 胃癌を対象としたDS-8201a(trastuzumabderuxtecan)の第Ⅲ相試験 | ||
| 腫瘍内科 | 胃癌又は食道胃接合部癌患者を対象としたAMG 552第III相試験 | ||
| 腫瘍内科 | MK-3475の治験に参加した進行悪性腫瘍患者を対象とした第Ⅲ相継続試験 | ||
| 腫瘍内科 | 胃癌又は食道胃接合部癌患者を対象としたAMG 552の第Ib/III相試験 | ||
| 医師主導治験 | 腫瘍内科 | HER2陽性の胃腺癌又は胃食道接合部腺癌患者を対象としたTrastuzumab Deruxtecan術前化学療法の第II相臨床試験 | |
| 腫瘍内科 | An Open-label Randomized Phase 3 Study of Tucatinib in Combination with Trastuzumab and mFOLFOX6 versus mFOLFOX6 given with or without either Cetuximab or Bevacizumab as First-line Treatment for Subjects with HER2+ Metastatic Colorectal Cancer HER2陽性転移性結腸直腸癌被験者を対象に、一次治療としてのトラスツズマブ及びmFOLFOX6併用tucatinibをセツキシマブ若しくはベバシズマブ併用又は非併用mFOLFOX6と比較する非盲検、無作為化、第3相試験 |
||
| 腫瘍内科 | 未治療のdMMR/MSI-H を有する切除可能な結腸癌患者を対象としたdostarlimab の第III 相試験 | ||
| 腫瘍内科 | HER2陽性転移性胃食道腺癌患者を対象としたZanidatamabとの化学療法併用の第Ⅲ相試験 | ||
| 腫瘍内科 | 胃がんを対象としたONO-4578の第Ⅱ相試験 | ||
| 膠原病・リウマチ内科 | 全身性エリテマトーデス患者を対象としたBIIB059の第Ⅲ相試験 | ||
| 膠原病・リウマチ内科 | 好酸球性多発血管炎性肉芽腫症における神経障害に対するGB-0998の有効性、安全性を検討する多施設共同オープン試験 | ||
| 膠原病・リウマチ内科 | 活動性ループス腎炎患者を対象としたRO5072759の第III相試験 | ||
| 精神・神経科 | 早期症候性アルツハイマー病を対象としたLY3002813の第Ⅲ相試験 | ||
| 精神・神経科 | 早期症候性アルツハイマー病を対象としたLY3372689の第Ⅱ相試験 | ||
| 精神・神経科 | LY3372993の第Ⅲ相試験 | ||
| 小児科 | 好酸球性重症喘息患者を対象としたGSK3511294をメポリズマブ又はベンラリズマブと比較評価する非劣性試験 | ||
| 乳腺外科 | Phase III Study of Trastuzumab Deruxtecan (T-DXd) with or without Pertuzumab versus Taxane, Trastuzumab and Pertuzumab in HER2-positive, First-line Metastatic Breast Cancer (DESTINY-Breast09) HER2陽性の転移性乳癌に対する一次治療としてトラスツズマブ デルクステカン(T-DXd)の単剤投与またはT-DXdとペルツズマブの併用投与と、タキサン、トラスツズマブ、及びペルツズマブの併用療法を比較検討する第III相試験(DESTINY-Breast09試験) |
||
| 医師主導治験医療機器 | 脳神経外科 | 慢性期脳梗塞(脳梗塞発症後150日以降365日以内)患者に対するMB-001(CD34陽性細胞分離機器)を用いた自家末梢血CD34陽性細胞の内頚動脈内投与に関する医師主導治験 詳しい情報はjRCTをご覧ください。 |
|
| 脳神経外科 | 急性期虚血性脳卒中又は高リスク一過性脳虚血発作後の脳卒中の再発抑制を目的とした経口第XIa因子阻害剤Milvexianの有効性及び安全性を評価する第3相,ランダム化,二重盲検,並行群間,プラセボ対照試験 | ||
| 医師主導治験 | 脳神経外科 | 脳動脈瘤に対するフローダイバーター( PFMD 001 )の有効性及び安全性を検証する多施設共同単一群試験 | |
| 医師主導治験 | 脳神経外科 | ダイレーターを用いた急性虚血性脳卒中に対する再開通療法の安全性及び有効性を評価する多施設共同単一群試験 | |
| 泌尿器科 | 根治的前立腺全摘除術の候補である高リスクかつ限局性又は局所進行性前立腺癌を対象としたapalutamideの第Ⅲ相試験 | ||
| 泌尿器科 | 去勢抵抗性前立腺癌を対象としたMK-7339の第Ⅲ相試験 | ||
| 泌尿器科 | 転移性ホルモン感受性前立腺癌を対象としたAZD5363の第Ⅲ相試験 | ||
| 泌尿器科 | 転移性去勢抵抗性前立腺癌患者を対象としたLY2835219の第Ⅱ/Ⅲ相試験 | ||
| 泌尿器科 | 前立腺がんを対象としたAAA617の第Ⅲ相試験 | ||
| 泌尿器科 | AAA617の第Ⅱ相試験 | ||
| 泌尿器科 | ハイリスクの転移性ホルモン感受性前立腺癌男性患者を対象としたLY2835219の第Ⅲ相試験 | ||
| 泌尿器科 | 前立腺がんを対象としたAZD5363の第Ⅲ相試験 | ||
| 泌尿器科 | 腎細胞癌患者を対象としたMK-6482の第Ⅲ相試験 | ||
| 泌尿器科 | カルメット・ゲラン桿菌(BCG)未治療の高リスク筋層非浸潤 性 膀胱癌(HR-NMIBC)患者を対象に,TAR-200 と cetrelimab の併用投与又は TAR-200 単独投与と,BCG 膀胱内投与の有効性及び安全性を比較する,第 3 相非盲検多施設共同ランダム化試験 | ||
| 医師主導治験 | 泌尿器科 | 筋層浸潤性膀胱癌に対するMK-3475(ペムブロリズマブ)の第Ⅱ相試験 | |
| 泌尿器科 | AAA617 の第Ⅲ相試験 | ||
| 泌尿器科 | 転移性去勢感受性前立腺癌患者を対象としたAZD5305の第III相試験 | ||
| 泌尿器科 | 感受性FGFR遺伝子異常を有する中リスク筋層非浸潤性膀胱癌(IR-NMIBC)患者を対象に,erdafitinib膀胱内送達システムであるTAR-210の有効性及び安全性を単剤膀胱内化学療法と比較して評価する第3 相ランダム化試験 | ||
| 腎臓内科 | IgA腎症患者を対象としたVR-205の第Ⅲ相試験 | ||
| 腎臓内科 | 免疫グロブリンA腎症(IgA腎症)を対象としたラブリズマブの第3相試験 | ||
| 放射線診断科 | Efficacy and safety of gadopiclenol for Magnetic Resonance Imaging (MRI) in Japanese adults and children Phase III Clinical Trial 日本人成人及び小児を対象とした磁気共鳴画像法(MRI)におけるgadopiclenolの有効性及び安全性を評価する第III相試験 |
||
| 産婦人科 | 進行卵巣癌を対象としたオラパリブ/デュルバルマブの第Ⅲ相試験 | ||
| 医師主導治験 | 産婦人科 | 子宮内膜異型増殖症・子宮体癌に対するメドロキシプロゲステロンとメトホルミンの併用妊孕性温存療法の用量反応性試験 | |
| 医師主導治験 | 心臓血管外科 | 経食道運動誘発電位ならびに測定に用いる経食道脊髄刺激電極の有効性及び安全性を検討する第 Ⅲ相試験 | |
| 麻酔科 | 持続的血液浄化療法(CBP)を施行する患者を対象としたWBCRRD及びSPB-KTの第Ⅲ相臨床評価 |
- 神戸大学医学部附属病院
| 治験種別 | 疾患領域 | 試験名・適応症 | 備考 |
| 皮膚科 | 尋常性白斑の試験 |
- 兵庫県立こども病院
| 治験種別 | 疾患領域 | 試験名・適応症 | 備考 |
| 血液腫瘍内科 | 日本イーライリリー株式会社の依頼によるアベマシクリブ(LY2835219)の第Ⅱ相試験 | 院内 | |
| 血液腫瘍内科 | 小児・AYA世代に好発する悪性腫瘍に対するシスプラチン投与による内耳毒性を軽減するチオ硫酸ナトリウムの第Ⅱ相試験(医師主導治験) | 院内 | |
| 腎臓内科 | 小児期発症のネフローゼ症候群早期再発例における IDEC-C2B8 投与の有効性の検討 -多施設共同ランダム化並行群間比較試験(JSKDC12)-(医師主導治験) | 院内 | |
| 神経内科 | 中外製薬株式会社の依頼による抗NMDAR脳炎又は抗LGI1脳炎患者を対象としたサトラリズマブの第Ⅲ相試験 | 院内 | |
| 代謝内分泌内科 | 軟骨無形成症の小児を対象とした観察試験 | 院内 | |
| リウマチ科 | アッヴィ合同会社の依頼による ABT-494(Upadacitinib)の多施設共同、無作為化、非盲検試験 | 院内 | |
| リウマチ科 | シミック株式会社(治験国内管理人)の依頼による日本人のスチル病(SJIA 及びAOSD)患者を対象としたanakinraの第III相試験 | 院内 | |
| 血液腫瘍内科 | インヒビターを保有しない血友病A及びB患者を対象としたconcizumabの予防治療における有効性及び安全性の検討 | 小児治験ネットワーク | |
| 血液腫瘍内科 | アレクシオンファーマ合同会社の依頼による造血幹細胞移植(HSCT)後に血栓性微小血管症(TMA)を呈する小児患者を対象としたラブリズマブの第III相試験 | 小児治験ネットワーク | |
| 血液腫瘍内科 | ファイザー株式会社の依頼によるインヒビター保有または非保有の小児血友病患者を対象としたmarstacimab定期投与第3相試験 | 小児治験ネットワーク | |
| 血液腫瘍内科 | ノバルティスファーマ株式会社の依頼によるCTL019の第IIIb相試験 | 小児治験ネットワーク | |
| 血液腫瘍内科 | 武田薬品工業株式会社の依頼による小児及び青年期の造血幹細胞移植(HSCT)患者又は固形臓器移植(SOT)患者におけるサイトメガロウイルス(CMV)感染 /感染症を対象としたTAK-620の第3相試験 | 小児治験ネットワーク | |
| 血液腫瘍内科 | 小児再発急性骨髄性白血病に対してフルダラビン+シタラビン+ゲムツズマブオゾガマイシンにベネトクラクス併用の有無を検証するランダム化比較第III相試験(医師主導治験) | 小児治験ネットワーク | |
| 腎臓内科 | アストラゼネカ株式会社の依頼による小児の高カリウム血症を対象としたSZCの第3相臨床試験 | 小児治験ネットワーク | |
| 代謝内分泌内科 | 2歳又はそれ以上の年齢においても成長のcatch-upがみられなかったSmallfor Gestational Age性低身長症患児を対象として、somapacitanの週1回投与の有効性及び安全性を1日1回投与のNorditropin®と比較検討する用量設定試験 | 小児治験ネットワーク | |
| 代謝内分泌内科 | PRAヘルスサイエンス株式会社の依頼による日本人小児成長ホルモン分泌不全性低身長症患者を対象としたlonapegsomatropinの第3相試験 | 小児治験ネットワーク | |
| 代謝内分泌内科 | Small for Gestational Age 性低身長症、ターナー症候群における低身長、ヌーナン症候群における低身長又は特発性低身長症の患児を対象として、週1回投与のソマプシタンの効果及び安全性を1日1回投与のノルディトロピン®と比較し、ソマプシタンの長期安全性を評価するバスケット試験 | 小児治験ネットワーク | |
| リウマチ科 | アッヴィ合同会社の依頼による ABT-494(Upadacitinib)の第I相試験 | 小児治験ネットワーク | |
| 心臓血管外科 | バクスター株式会社の依頼による小児先天性心疾患患者を対象としたBAX602の安全性及び有効性に関する試験 | 小児治験ネットワーク | |
| 血液腫瘍内科 | 初発の中間リスク急性リンパ芽球性白血病を有する0から24才の被験者を対象に標準的な強化療法とブリナツモマブを追加した強化療法の有効性と安全性を比較するオープンラベル、ランダム化、第2相、2群試験(医師主導治験) | 東北臨床研究審査機構 |
- 神戸低侵襲がん医療センター
| 治験種別 | 疾患領域 | 試験名・適応症 | 備考 |
| 企業治験 | MSD株式会社の依頼による非小細胞肺がん患者を対象としたMK-3475/MK-7339の第Ⅲ相試験 | ||
| 企業治験 | MSD株式会社の依頼による小細胞肺がん患者を対象としたMK-3475/MK-7339の第Ⅲ相試験 | ||
| 企業治験 | 大鵬薬品工業株式会社の依頼による TAS-120 の第 1b相試験 | ||
| 企業治験 | アストラゼネカ株式会社の依頼による非小細胞肺がん患者を対象としたSavolitinibの第Ⅲ相試験 | ||
| 企業治験 | アッヴィ合同会社の依頼によるTelisotuzumab Vedotin(ABBV-399)の第Ⅱ相試験 | ||
| 企業治験 | MSD株式会社の依頼による非小細胞肺がん患者を対象としたMK-7684Aの第Ⅲ相試験 | ||
| 企業治験 | アッヴィ合同会社の依頼によるTelisotuzumab Vedotin(ABBV-399)の第Ⅲ相試験 | ||
| 企業治験 | アムジェン株式会社の依頼による肺がん患者を対象としたAMG 510(ソトラシブ)の第Ⅲ相試験 | ||
| 企業治験 | 転移性非扁平上皮非小細胞肺癌患者を対象に、SB27(ペムブロリズマブのバイオ後続品候補)とキイトルーダの有効性、安全性、薬物動態及び免疫原性を比較する第III相、無作為化、二重盲検、多施設共同試験 | ||
| 企業治験 | アストラゼネカ株式会社の依頼によるEGFR変異を有する局所進行又は転移性非小細胞肺癌患者を対象にオシメルチニブ併用/非併用下でのDato-DXdの有効性及び安全性を白金製剤を含む2剤併用化学療法と比較する試験 |
- 神戸市立神戸アイセンター病院
| 治験種別 | 疾患領域 | 試験名・適応症 | 備考 |
| 眼科 | nAMD患者を対象としたABBV-RGX-314の第Ⅲ相試験 | アッヴィ合同会社 | |
| 眼科 | Stargardt病患者を対象としたtinlarebantの第Ib相および第II/III相試験 | Belite Bio, Inc | |
| 眼科 | 原発開放隅角緑内障又は高眼圧症患者を対象としたSJP-0170の実薬対照比較試験 | 千寿製薬株式会社 |
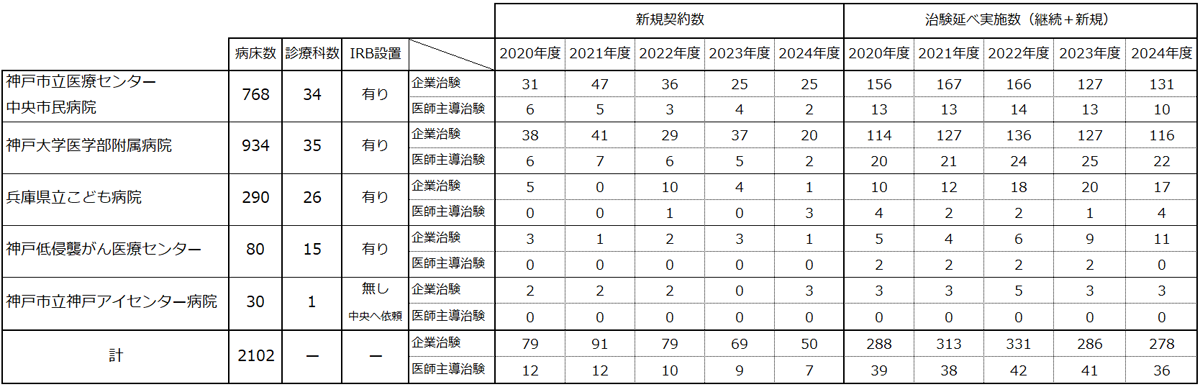
治験実績 ※2024年12月末時点
手順書・書類集リンク
| 施設名 | 病床数 | 診療科数 | IRB(治験審査委員会)設置 | 手順書・申請書リンク | 治験実績リンク | 問い合わせ先 |
| 神戸市立医療センター中央市民病院 | 768 | 34 | 有り | 施設の専用ページへ | 施設の専用ページへ | 施設の専用ページへ |
| 神戸大学医学部附属病院 | 934 | 35 | 有り | 施設の専用ページへ | 施設の専用ページへ | 施設の専用ページへ |
| 兵庫県立こども病院 | 290 | 26 | 有り | 施設の専用ページへ |
施設の専用ページへ
※トップページ右上 |
|
| 神戸低侵襲がん医療センター | 80 | 15 | 有り | 施設の専用ページへ |
施設の専用ページへ
※リンク先ページ最下部 |
|
| 神戸市立神戸アイセンター病院 | 30 | 1 |
無し
※神戸市立医療センター 中央市民病院へ依頼 |
施設の専用ページへ
※神戸市立医療センター 中央市民病院リンク |
施設の専用ページへ |